Нейродегенеративные заболевания головного мозга и нервной системы
Ранняя диагностика нейродегенеративных заболеваний
С.Н. Иллариошкин
доктор медицинских наук, профессор, заместитель директора по научной работе
ГУ Научный центр неврологии РАМН
Термином нейродегенеративные заболевания” определяется большая группа заболеваний преимущественно позднего возраста, для которых характерна медленно прогрессирующая гибель определенных групп нервных клеток и одновременно – постепенно нарастающая атрофия соответствующих отделов головного и/или спинного мозга. Наиболее известными представителями этого класса заболеваний человека являются болезни Альцгеймера, Паркинсона, Гентингтона, Пика. Поскольку в развитых странах мира наблюдается неуклонное старение населения, общая частота нейродегенеративных заболеваний имеет четкую тенденцию к увеличению. Достаточно сказать, что у людей старше 70 лет распространенность этих заболеваний составляет около 5%, а среди лиц старше 80 лет – уже 10-15%; число пациентов только с болезнью Альцгеймера в мире превышает 30 млн. При этом следует помнить, что указанные страдания затрагивают как психику человека (потеря памяти и в конечном счете деменция при болезни Альцгеймера), так и его способности двигаться и обслуживать себя (скованность, дрожание, расстройства ходьбы при болезни Паркинсона). Таким образом, социальная значимость данной проблемы очевидна.
К сожалению, для большинства нейродегенеративных болезней отсутствуют радикальные методы лечения, которые позволили бы полностью остановить патологический процесс и тем более обратить его вспять. Возможности симптоматической помощи таким пациентам ограничены, причем в поздних стадиях лечение особенно затруднено и нередко сопровождается многочисленными осложнениями, которые нередко могут быть даже “хуже” самой болезни. Например, применение в поздней стадии болезни Паркинсона лекарств, восполняющих дефицит двигательных импульсов в мозгу, может из-за патологической реактивности нервных клеток привести к превращению малоподвижного пациента в “танцующего маньяка”, не способного ни на минуту остановиться (это чревато полным истощением, падениями, травмами и т.п.).
Где же выход? Как общество может эффективно противостоять этим, в буквальном смысле слова, “болезням века”?
Согласно современным представлениям, ключевое значение в стратегии борьбы с нейродегенеративными заболеваниями придается максимально ранней диагностике патологического процесса и в особенности – диагностике болезни в ее латентной стадии (синонимы – доклиническая, пресимптоматическая стадия). Латентная стадия означает, что на клеточном и молекулярном уровне болезнь уже началась и определенная часть нейронов уже погибла, но человек пока не ощущает себя больным и со стороны может выглядеть “в полном порядке”. Причем “запас прочности” центральной нервной системы весьма высок: например, боковой амиотрофический склероз манифестирует лишь когда свыше 50% двигательных нейронов спинного мозга перестают функционировать, а болезнь Паркинсона входит в клиническую стадию лишь после гибели более 70% нейронов среднего мозга, ответственных за двигательные функции. Всё, что происходит на более раннем этапе – это латентная фаза болезни.
Данные многочисленных клинических и экспериментальных исследований показывают, что при большинстве нейродегенеративных заболеваний латентная фаза длится в среднем около 6-8 лет, а затем сравнительно быстро развивается манифестация явных клинических проявлений болезни. Именно эти несколько лет составляют наиболее благоприятное “терапевтическое окно”, в течение которого необходимо стремиться диагностировать патологию и постараться вмешаться в неблагоприятный “сценарий” – предотвратить или хотя бы отсрочить наступление необратимых изменений.
Задача диагностики латентной стадии нейродегенерации базируется на двух нижеследующих составляющих.
1. Выделение факторов риска и формирование групп риска – лиц с высокой предрасположенностью к развитию болезни. Наиболее часто речь идет о генетических и средовых факторах риска той или иной болезни. Например, весьма значимым генетическим фактором риска болезни Альцгеймера является е4-вариант гена аполипопротеина Е (аполипопротеин Е отвечает за транспорт липидов и их “мобилизацию” при построении мембран нейронов): если человек имеет две копии такого гена, то у него риск развития болезни Альцгеймера в пожилом возрасте составляет свыше 90%. Иллюстрацией средовых факторов риска может служить выявленная взаимосвязь между частотой возникновения болезни Паркинсона и длительным, многолетним контактом с некоторыми пестицидами (что может иметь место у лиц, занятых в агрохимическом производстве).
2. Установление биомаркеров ранней и пресимптоматической стадии нейродегенеративного процесса. Биомаркеры – это различные лабораторно-инструментальные показатели состояния организма, которые могут “сигнализировать” о текущем неблагополучии (в том числе о неблагополучии со стороны центральной нервной системы). В неврологии наиболее перспективными считаются три группы биомаркеров:
• нейрофизиологические и нейропсихологические (изменение нормальной картины биоэлектрической активности мозга при электроэнцефалографии, тонкие изменения психики и профиля личности при использовании специальных тестов и др.);
• молекулярно-биохимические (например, повышение в цереброспинальной жидкости и крови пациентов уровня некоторых белков, строго специфичных для вещества мозга);
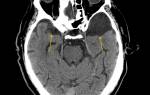
• нейровизуализационные (выявление с помощью специальных методик рентгеновской, магнитно-резонансной или радиоизотопной компьютерной томографии тех или иных функционально-биохимических изменений в веществе мозга либо тонких признаков нарастающего уменьшения объема отдельных ядер – скоплений нейронов в определенных отделах мозга).
Выявление у человека из группы риска одного или нескольких вышеуказанных маркеров нейродегенеративного процесса позволяет с высокой степенью вероятности (которую можно даже рассчитать специальными методами) диагностировать наличие латентной стадии болезни и поставить вопрос о проведении ранней терапии, направленной на предотвращение прогрессирования (нейропротекция). По существующим прогнозам, новые препараты с доказанным нейропротективным действием могут появиться в арсенале врачей-неврологов уже в самые ближайшие годы, и мы обязательно затронем эту проблему в будущих номерах журнала.
Ранняя диагностика нейродегенеративных заболеваний
С.Н. Иллариошкин
доктор медицинских наук, профессор, заместитель директора по научной работе
ГУ Научный центр неврологии РАМН
Термином нейродегенеративные заболевания” определяется большая группа заболеваний преимущественно позднего возраста, для которых характерна медленно прогрессирующая гибель определенных групп нервных клеток и одновременно – постепенно нарастающая атрофия соответствующих отделов головного и/или спинного мозга. Наиболее известными представителями этого класса заболеваний человека являются болезни Альцгеймера, Паркинсона, Гентингтона, Пика. Поскольку в развитых странах мира наблюдается неуклонное старение населения, общая частота нейродегенеративных заболеваний имеет четкую тенденцию к увеличению. Достаточно сказать, что у людей старше 70 лет распространенность этих заболеваний составляет около 5%, а среди лиц старше 80 лет – уже 10-15%; число пациентов только с болезнью Альцгеймера в мире превышает 30 млн. При этом следует помнить, что указанные страдания затрагивают как психику человека (потеря памяти и в конечном счете деменция при болезни Альцгеймера), так и его способности двигаться и обслуживать себя (скованность, дрожание, расстройства ходьбы при болезни Паркинсона). Таким образом, социальная значимость данной проблемы очевидна.
К сожалению, для большинства нейродегенеративных болезней отсутствуют радикальные методы лечения, которые позволили бы полностью остановить патологический процесс и тем более обратить его вспять. Возможности симптоматической помощи таким пациентам ограничены, причем в поздних стадиях лечение особенно затруднено и нередко сопровождается многочисленными осложнениями, которые нередко могут быть даже “хуже” самой болезни. Например, применение в поздней стадии болезни Паркинсона лекарств, восполняющих дефицит двигательных импульсов в мозгу, может из-за патологической реактивности нервных клеток привести к превращению малоподвижного пациента в “танцующего маньяка”, не способного ни на минуту остановиться (это чревато полным истощением, падениями, травмами и т.п.).
Где же выход? Как общество может эффективно противостоять этим, в буквальном смысле слова, “болезням века”?
Согласно современным представлениям, ключевое значение в стратегии борьбы с нейродегенеративными заболеваниями придается максимально ранней диагностике патологического процесса и в особенности – диагностике болезни в ее латентной стадии (синонимы – доклиническая, пресимптоматическая стадия). Латентная стадия означает, что на клеточном и молекулярном уровне болезнь уже началась и определенная часть нейронов уже погибла, но человек пока не ощущает себя больным и со стороны может выглядеть “в полном порядке”. Причем “запас прочности” центральной нервной системы весьма высок: например, боковой амиотрофический склероз манифестирует лишь когда свыше 50% двигательных нейронов спинного мозга перестают функционировать, а болезнь Паркинсона входит в клиническую стадию лишь после гибели более 70% нейронов среднего мозга, ответственных за двигательные функции. Всё, что происходит на более раннем этапе – это латентная фаза болезни.
Данные многочисленных клинических и экспериментальных исследований показывают, что при большинстве нейродегенеративных заболеваний латентная фаза длится в среднем около 6-8 лет, а затем сравнительно быстро развивается манифестация явных клинических проявлений болезни. Именно эти несколько лет составляют наиболее благоприятное “терапевтическое окно”, в течение которого необходимо стремиться диагностировать патологию и постараться вмешаться в неблагоприятный “сценарий” – предотвратить или хотя бы отсрочить наступление необратимых изменений.
Задача диагностики латентной стадии нейродегенерации базируется на двух нижеследующих составляющих.
1. Выделение факторов риска и формирование групп риска – лиц с высокой предрасположенностью к развитию болезни. Наиболее часто речь идет о генетических и средовых факторах риска той или иной болезни. Например, весьма значимым генетическим фактором риска болезни Альцгеймера является е4-вариант гена аполипопротеина Е (аполипопротеин Е отвечает за транспорт липидов и их “мобилизацию” при построении мембран нейронов): если человек имеет две копии такого гена, то у него риск развития болезни Альцгеймера в пожилом возрасте составляет свыше 90%. Иллюстрацией средовых факторов риска может служить выявленная взаимосвязь между частотой возникновения болезни Паркинсона и длительным, многолетним контактом с некоторыми пестицидами (что может иметь место у лиц, занятых в агрохимическом производстве).
2. Установление биомаркеров ранней и пресимптоматической стадии нейродегенеративного процесса. Биомаркеры – это различные лабораторно-инструментальные показатели состояния организма, которые могут “сигнализировать” о текущем неблагополучии (в том числе о неблагополучии со стороны центральной нервной системы). В неврологии наиболее перспективными считаются три группы биомаркеров:
• нейрофизиологические и нейропсихологические (изменение нормальной картины биоэлектрической активности мозга при электроэнцефалографии, тонкие изменения психики и профиля личности при использовании специальных тестов и др.);
• молекулярно-биохимические (например, повышение в цереброспинальной жидкости и крови пациентов уровня некоторых белков, строго специфичных для вещества мозга);
• нейровизуализационные (выявление с помощью специальных методик рентгеновской, магнитно-резонансной или радиоизотопной компьютерной томографии тех или иных функционально-биохимических изменений в веществе мозга либо тонких признаков нарастающего уменьшения объема отдельных ядер – скоплений нейронов в определенных отделах мозга).
Выявление у человека из группы риска одного или нескольких вышеуказанных маркеров нейродегенеративного процесса позволяет с высокой степенью вероятности (которую можно даже рассчитать специальными методами) диагностировать наличие латентной стадии болезни и поставить вопрос о проведении ранней терапии, направленной на предотвращение прогрессирования (нейропротекция). По существующим прогнозам, новые препараты с доказанным нейропротективным действием могут появиться в арсенале врачей-неврологов уже в самые ближайшие годы, и мы обязательно затронем эту проблему в будущих номерах журнала.
Нейродегенеративные заболевания
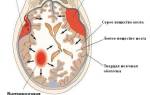
- мозг
- позвоночник
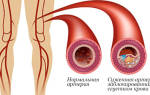
- нервы и сосуды
1. Что включает группа нейродегенеративных заболеваний?
Термин «нейродегенеративные заболевания» охватывает всю совокупность расстройств, обусловленных дегенеративными изменениями элементов нервной системы – мозга и проводящих нервов. Для любой патологии этого типа свойственна тесная связь органических и функциональных нарушений, причём характер последних определяется локализацией патологического процесса и степенью атрофии тканей тех или иных отделов мозга.
Нейродегенеративные заболевания (НДЗ) приводят к постепенному нарастанию психической и физической несостоятельности. Прогрессирующая патология головного мозга как центра регуляции приводит к когнитивным и двигательным расстройствам. При этом на начальных этапах сохраняется критика, что влечёт тяжелые переживания больного от осознания собственной ущербности. Комплекс прогрессирующих нарушений при НДЗ может включать:
- поведенческие расстройства;
- двигательные нарушения;
- утрату памяти, мышления;
- угасание способности к восприятию и осмыслению;
- нарушения речи;
- дисбаланс в эмоционально-волевой сфере.
Нейродегенеративные заболеваниям свойственно прогрессирование, приводящее к дегенерации личности, полной утрате трудоспособности и дееспособности. Как правило, смерть пациентов наступает по истечении нескольких (иногда десятков) лет от присоединившихся заболеваний, что отчасти можно связать с возрастающими трудностями в уходе и обслуживании таких больных.
2. Причины нейродегенеративных заболеваний и факторы риска
Точная причина, провоцирующая начало патологии, ни для одного нейродегенеративного заболевания не выявлена. Отмечаются некоторые характерные фоновые состояния, присущие в том или ином сочетании больным НДЗ. Наиболее часто выявляются следующие тенденции:
- сбои в метаболизме и синтезе некоторых белков, составляющих миелиновую оболочку нейронов (их нехватка или излишнее накопление);
- нарушения деятельности рецепторов структур мозга, связанных с нейромедиаторным регулированием;
- генетическая предрасположенность, наличие родственников с нейродегенеративными заболеваниями;
- интоксикация и гибель нейронов на фоне сопутствующих патологических процессов или под действием постоянно действующих негативных факторов (свободных радикалов, гербицидов, пестицидов, алкоголя и наркотических веществ).
Кроме того, косвенными факторами риска признаны многие затрагивающие обменные процессы патологии:
- инфекции;
- ожирение;
- травмы головы;
- заболевания сердечно-сосудистой системы;
- хронические эндокринные нарушения;
- почечная и печёночная недостаточность как механизм вывода токсинов;
- все вредные привычки;
- низкая физическая и интеллектуальная активность.
3. Диагностика и клиническая картина при нейродегенеративных заболеваниях
На начальных этапах различные НДЗ могут иметь схожую клиническую картину. Диагностика должна основываться не только на сборе анамнестических данных и динамическом наблюдении, а также затрагивать генетические аспекты. Дифференцировать конкретный диагноз помогают специальные тесты. Для исключения опухолевого, травматического, сосудистого генеза начавшихся нарушений применяются инструментальные методы диагностики.
Наиболее показательны следующие методики обследования при подозрении на НДЗ:
- МРТ, КТ головного мозга;
- ПЭТ;
- однофотонная КТ;
- исследование уровня нейромедиаторов;
- ангиография;
- УЗДГ сосудов головного мозга и шейного отдела;
- ЭЭГ.
Клинические проявления нейродегенеративных заболеваний зависят от стадии и определённого вида патологии. Чаще всего симптомокомплекс включает двигательные нарушения (изменение походки, тремор, акинезию и ригидность). Часто по мере прогрессирования болезни развивается постуральная неустойчивость. Возможны гиперкинезы, самопроизвольные или насильственные движения.
В уровне интеллекта имеет место деменция, ослабление памяти, мыслительной деятельности, нарушаются контакты с окружающими. Как следствие – больной человек постепенно самоизолируется. Для постановки диагноза часто показательным является факт первичности нарушений двигательной активности или интеллекта. Сохранной остаётся мышечная активность на начальных стадиях болезни Альцгеймера, при сосудистой деменции, болезни Пика. Тогда как болезнь Паркинсона, Хорея Гентингтона изначально проявляются изменениями в походке, тремором, гиперкинезами.
4. Течение болезни и уход за больными НДЗ
Неуклонное прогрессирование заболеваний, связанных с нейродегенерацией, приводит таких больных к инвалидности. Они подвержены не только расстройствам интеллекта, памяти и мышления, но и беззащитны перед нарастающими двигательными нарушениями. Утрата здоровой координации движений нередко приводит к травмам. Вегетативная нервная система под «руководством» больного мозга начинает сбоить, приводя к расстройствам пищеварения, сухости кожи, запорам, нарушению мочеиспускания.
Дееспособность больных нейродегенеративными заболеваниями также всегда является спорным вопросом. Многие из них способны на асоциальные поступки и представляют угрозу для самих себя и окружающих.
Лечение НДЗ всегда неспецифическое и направлено на оказание симптоматической помощи, осуществление должного ухода за больным, сохранение как можно более длительно способности пациента взаимодействовать с теми, кто берёт его под свою опеку. На более тяжёлых стадиях основные задачи – кормление, гигиена, профилактика инфекций и травм, а также пролежней и иных осложнений.